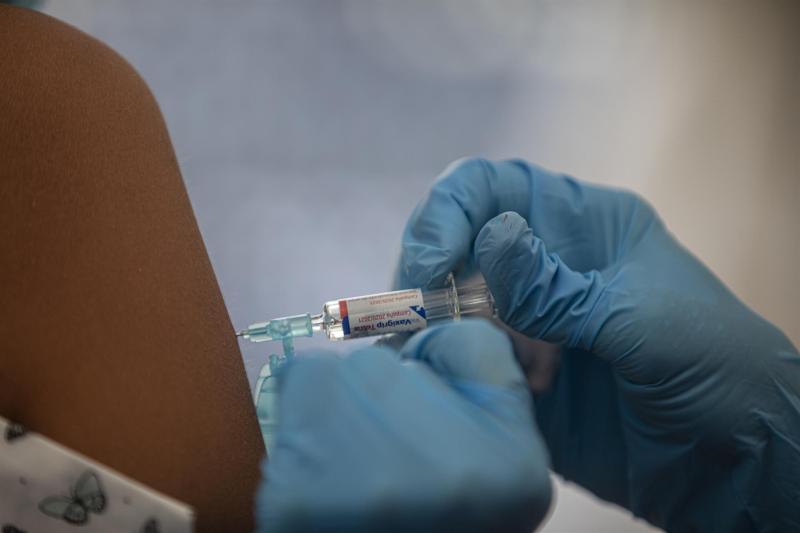
La cap del servei de medicina preventiva i epidemiologia de l'Hospital Vall d'Hebron de Barcelona, Magda Campins, ha explicat que el centre ha començat el reclutament de voluntaris per participar en l'assaig clínic en fase 3 de la vacuna contra el Covid-19 de la farmacèutica Janssen.
En roda de premsa aquest dimecres al costat de les altres responsables de l'assaig al centre català Susana Otero i Ingrid Carbonés, Campins ha concretat que es tracta del "primer assaig d'aquestes característiques" que s'ha autoritzat en l'Estat.
Aquest dimecres han començat el reclutament --que han estimat que finalitzarà en tres mesos aproximadament-- i Campins ha precisat que la previsió del centre és començar a vacunar la primera setmana de gener a mesura que vagin reclutant, també, més voluntaris.
L'Agència Espanyola de Medicaments i Productes Sanitaris (Aemps) va autoritzar el novembre passat l'assaig per avaluar "l'eficàcia i la seguretat" de la vacuna tant en voluntaris sans com en participants amb malalties que s'associen a un major risc de progressió a Covid-19 greu.
Aquest assaig inclourà fins a 30.000 voluntaris de nou països diferents --Bèlgica, Colòmbia, França, Alemanya, Sud-àfrica, Filipines, Espanya, el Regne Unit i els Estats Units-- i en el qual a més del centre català, que espera aportar 200 voluntaris, participen altres set hospitals de l'Estat.
En concret, aquests centres són: l'Hospital Clínic de Barcelona, l'Hospital Quirónsalud de Barcelona, l'Hospital Germans Trias i Pujol de Badalona (Barcelona), l'Hospital de la Princesa de Madrid, l'Hospital la Pau de Madrid, l'Hospital Quirónsalud de Madrid i la Clínica Universidad de Navarra.
PERFIL DELS VOLUNTARIS
Sobre el perfil dels voluntaris, les doctores han precisat que no podran participar en l'assaig persones inmunodeprimides per una malaltia de base o bé en tractament amb medicaments inmunosupresors.
Tampoc es permet la participació de dones embarassades o amb probabilitat d'embaràs en els dos propers anys, persones amb antecedents d'anafilaxia o reaccions adverses greus a les vacunes ni persones que ja participin en altres assajos clínics.
En coincidir amb el desplegament de la campanya de vacunació, Campins ha lamentat que hi haurà persones que s'havien presentat voluntàries que sortiran de l'assaig perquè no poden participar si els administren la vacuna.
El grup en el qual hi ha "més persones que sortiran" de l'assaig serà el dels professionals sanitaris perquè són un col·lectiu prioritari dins de l'estratègia de vacunació i, segons Campins, decidiran lògicament no participar.
ASSAIG
La vacuna, amb el nom Ad26.COV2.S, no conté el virus viu sinó que utilitza una proteïna artificial del virus perquè l'organisme generi anticossos.
L'estudi és randomitzat, doble cec i controlat amb placebo, és a dir, de manera aleatòria se'ls administrarà a la meitat dels participants la dosi mentre que l'altra meitat rebrà el placebo.
A més, el placebo serà emmascarat pel que ni el personal sanitari ni els voluntaris podran identificar quin producte s'està administrant.
Aquest assaig estudiarà "la seguretat i l'eficàcia" en un règim de dues dosis de la vacuna que s'injectaran amb 57 dies de diferència entre la primera i la segona dosi, i es farà un seguiment dels voluntaris durant dos anys.
SEGUIR DESENVOLUPANT VACUNES
Campins ha defensat que és "imprescindible" seguir desenvolupant altres vacunes candidates per poder garantir una major disponibilitat i també poder perfilar estratègies ajustades a cada grup poblacional segons el tipus de vacuna.
Ha concretat que pot ser que hi hagi vacunes que tinguin una "major efectivitat" en persones d'edat avançada i altres més efectives en gent amb patologies de base, entre uns altres.